Secondo uno studio epidemiologico del 1986 il cheratocono colpisce circa uno su 1.800 individui (1) (ed è per questo che rientra ancora tra le malattie rare), ma da quella data gli sviluppi tecnologici hanno comportato cambiamenti sostanziali nella sua diagnosi e gestione.
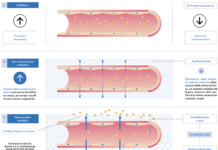
Le possibilità diagnostiche si sono talmente sviluppate da consentirci potenzialmente di individuare forme fruste subcliniche di cheratocono e, di conseguenza, l’incidenza non dovrebbe più essere quella sopra descritta ma ben maggiore, fino a 5-10 volte maggiore come evidenziato in uno studio epidemiologico olandese (2). Inoltre, da allora sono state introdotte non solo tecniche di trattamento per forme evolute di cheratocono, ma soprattutto tecniche parachirurgiche (crosslinking CXL) di contenimento della progressione del cheratocono, tanto più efficaci e di soddisfazione per la visione del paziente quanto prima effettuabili in forme non evolute.
Ora che abbiamo la capacità di rallentare o forse persino di fermare la progressione (con CXL), l'obiettivo cambia dal tentativo di migliorare la visione già ridotta alla prevenzione di una diminuzione della visione; ecco perché nella nostra pratica clinica ambulatoriale l’attenzione all’identificazione precoce o all’invio per diagnosi topografiche dei casi che ci appaiono (anche solo) sospetti appare fondamentale, in modo da far giungere i pazienti ai centri attrezzati per tempestivi protocolli di cura, in base alle condizioni cliniche di ciascun paziente e alle possibilità terapeutiche e alla disponibilità di ciascun centro. Nondimeno, dobbiamo essere ben informati e consci di quello che avviene a seguito dei trattamenti conservativi (CXL) per poter noi stessi seguire il paziente nel suo percorso di follow up, postoperatorio e riabilitativo all’interno della continuità assistenziale ospedale – territorio.
Il cheratocono è un disturbo progressivo, verosimilmente non infiammatorio, ectasico della cornea, che parte dalla sua superficie posteriore, ed è caratterizzato da una diminuzione dello spessore corneale e da una crescente curvatura corneale solo talora centrale, ma più spesso para o pericentrale, in genere inferiore, inferotemporale, temporale o eccezionalmente superiore. In alcune occasioni si manifesta periferico inferiore (degenerazione pellucida) con un astigmatismo più o meno regolare contro regola.
Tutto ciò coincide con un aumento dell'irregolarità corneale e delle aberrazioni di ordine superiore (in particolare coma e trefoil, ma anche aberrazione sferica), che si manifestano come una diminuzione della qualità visiva.
La maggior parte dei casi è bilaterale e asimmetrica. La malattia insorge di solito durante la pubertà o l'adolescenza e può progredire o meno (con decorso totalmente soggettivo e imprevedibile) fino ai 30-40 anni per poi arrestarsi spontaneamente; dopo i 40-45 anni si ha un cosiddetto CXL spontaneo con meno dello 0,4% dei casi in progressione, con particolare attenzione al rischio nella degenerazione marginale pellucida (rientrante nelle ectasie corneali, ma non sempre definita cheratocono).
Come detto, la progressione del cheratocono non dipende dalle condizioni cliniche e oculari e non è possibile definire una regola generale, per cui ogni caso deve essere visto individualmente. A volte il cheratocono progredisce rapidamente fino a 6 mesi/1 anno e poi si stabilizza per anni, per poi avere una nuova progressione. In altri pazienti si ha una progressione lenta e graduale per più di 10 anni. In generale, più precoce è l’insorgenza e con valori di K-max elevati al riscontro più aggressivo deve essere considerato il cheratocono (3).
Vorremmo tutti poter avere assieme all’autorefrattometro anche un topografo, possibilmente scheimpflung, nell'ambulatorio, ma in assenza di questo dobbiamo ricordare alcune accortezze nella nostra visita per poter avere perlomeno il dubbio della presenza di cheratocono.
Anamnesi e fattori di rischio
L’anamnesi, spesso dimenticata nella fretta di una visita ambulatoriale, è invece fondamentale per indirizzare a una maggiore attenzione diagnostica.
Infatti la prevalenza di cheratocono è più elevata nei soggetti con sindromi di Down, Marfan e Ehlers–Danlos, in quelli con prolasso valvolare mitralico (fino al 58% dei casi), atopia (presente nel 53% dei casi di cheratocono come eczema, raffreddore da fieno o asma) e in coloro che riportano una storia di strofinamento oculare anormale (“rubbing”, presente in quasi il 50% dei casi, definito statisticamente come fattore di rischio di progressione e da proscrivere agli affetti da cheratocono e a quelli a rischio).
Il cheratocono è stato anche collegato ad alcuni disturbi immunitari (tra cui artrite reumatoide, epatite cronica attiva autoimmune e sindrome del colon irritabile). La familiarità positiva è considerata un alto fattore di rischio, in quanto i figli di un paziente affetto da cheratocono presentano un rischio di malattia tra il 10 e il 30% rispetto allo 0,05% dei soggetti con genitori sani. Tuttavia, non sono stati identificati i geni responsabili della perdita di equilibrio di produzione/degradazione delle fibre di collagene dello stroma corneale sottoposte a forze di tensione con conseguente formazione di un "locus" di minore resistenza.
Il cheratocono deve sempre essere sospettato (non solo nei miopi ma anche negli ipermetropi) in caso di aumento dell'astigmatismo nel breve periodo (6-12 mesi), soprattutto con modifica dell’asse, un’improvvisa e ripetuta modifica del difetto refrattivo, una riduzione dell'acuità visiva corretta specie monolaterale non altrimenti spiegabile, la comparsa di intolleranza alla lente a contatto, la tendenza allo strofinamento prima non presente, una marcata sensibilità alla luce (fotofobia), la riferita percezione di luci con aloni "allungati e distorti" (ben rappresentati dopo la diagnosi dal point spread function in topoaberrometria), numerosi cambi di lenti senza mai essere soddisfatti della qualità visiva raggiunta, una "fatica visiva" (simile a quella dei pazienti affetti da astigmatismo non corretto), una diplopia monoculare, che si presentino in bambini (casi descritti anche da 4-5 anni d'età in forte familiarità), ma soprattutto in giovani adulti (tipicamente tra i 12 e i 25 anni); insorgenze tardive (25-40 anni) sono altresì possibili.
Nelle forme non precocissime anche l’osservazione di lievi distorsioni inferiori dei cerchi di alcuni autorefrattometri possono far sorgere un dubbio. Peraltro è dimostrato come la prescrizione di lenti nel cheratocono su indicazione autorefrattometrica non sia adeguata (restituisce valori significativamente più miopi di equivalente sferico, cilindri negativi più elevati ed ad assi impropri), per cui devono essere applicate specifiche modalità di studio della refrazione manifesta soggettiva.
La valutazione della sensibilità al contrasto consentirebbe un riconoscimento precoce di disfunzione visiva rispetto allo studio dell’acuità visiva ad alto contrasto, che nelle forme precoci (cosiddette fruste) può non essere alterata.
La schiascopia/retinoscopia può rivelare un riflesso irregolare a forbice (“scissoring”), che si accentua con l’aumentare della gravità del cheratocono e che presenta un’alta sensibilità e specificità nella distinzione tra normale e patologico (4); anche l’oftalmoscopia dei pazienti con cheratocono mostra un riflesso a gocciolina d'olio (“oil droplet reflex”, segno di Charleux). Un'irregolarità corneale può anche essere rilevata durante la cheratometria (angolo di Amsler), ma in genere solo in forme non precoci.
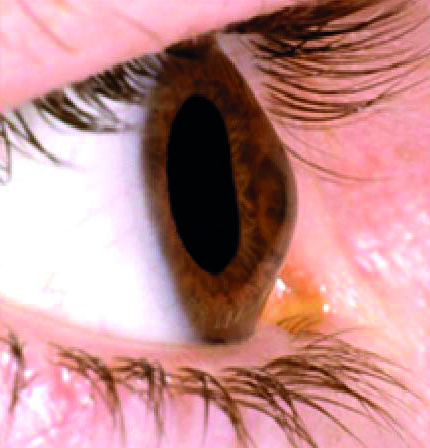
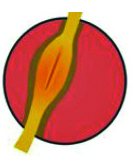
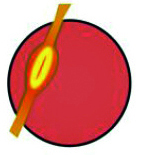
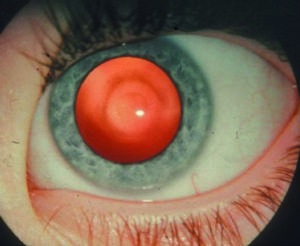
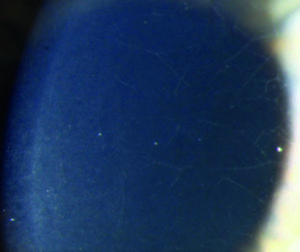
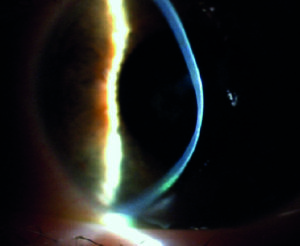
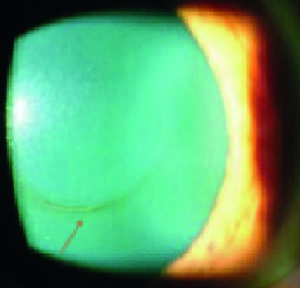
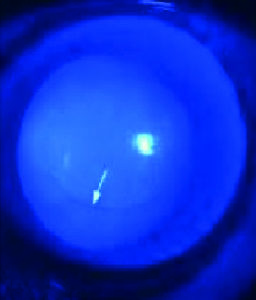
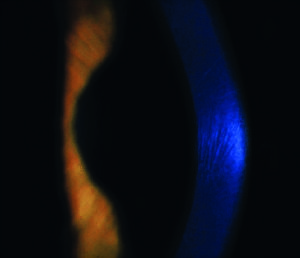
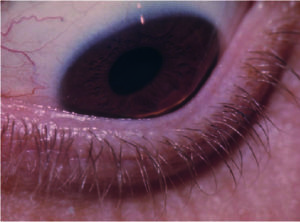
I segni rilevabili alla lampada a fessura variano con lo stadio della malattia e vanno da tenui segni precoci (ad esempio nervi corneali prominenti), al riconoscimento di un assottigliamento corneale all’apice del cono, all'emergere di un anello parziale o completo brunastro che delimita la base del cono (anello ferroso di Fleischer) e microstrie verticali corneali stromali profonde (strie di Vogt), che diventano man mano sempre più manifeste con il progredire della condizione. In casi avanzati l'irrigidimento corneale, l'assottigliamento e la cicatrizzazione apicali diventano evidenti, fino ad aversi il segno di Munson di spostamento palpebrale inferiore nello sguardo in basso per spiccata ectasia corneale (figura 1A. Retinoscopia: riflesso irregolare a forbice nei vari stadi della malattia).
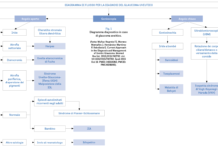
Diverse classificazioni che cercano di studiare il cheratocono sono state presentate, tra cui quella illustrata in tabella 1 (sotto). Va ricordato, tuttavia, che il cheratocono è uno spettro, i singoli casi potrebbero non adattarsi perfettamente a un singolo stadio della malattia.
| Forma | Acuità visiva corretta | K più curvo | Riflesso retinoscopico | Verosimili segni alla lampada a fessura |
| Frusta | 10/10 o meglio | 7.80-6.7 0mm (43.25-50-25 D) | Normale o appena irregolare | Normale o solo nervi corneali prominenti |
| Iniziale | 8/10 o meglio | 7.50-6.50 mm (45.00-52.00 D) | Progressivamente distorto | Minimo anello di Fleisher |
| Moderata | 3/10 – 9/10 | 6.90-5.30 mm (49-63.75 D) | Assottigliamento apicale, anello di Fleischer parziale o completo, iniziali strie di Vogt | |
| Avanzata | 1/10 – 6/10 | 6.60-4.80 mm (51.25-70-25 D) | Assottigliamento apicale, anello di Fleischer completo, strie di Vogt, possibili opacità apicali | |
| Molto avanzata | 1/20 – 2/10 | < 5.00 mm (> 67.50 D) | Spesso impossibile | Spesso opacità apicali, segno di Munson |
Tabella 1. Segni e sintomi possibili nelle forme progressive di cheratocono
L'importanza della diagnosi
Non abbiate paura di sbagliare nell’inviare un paziente nel dubbio di un cheratocono per l’effettuazione di una topografia e pachimetria; se verrà confermato avrete solo fatto il bene di quella persona, in quanto avrete verosimilmente evitato una possibile progressione di una malattia, che può significativamente ridurre la qualità di vita del paziente ed impatta negativamente anche sulle famiglie, che con la diagnosi di cheratocono percepiscono erroneamente ancora la paura di arrivare senza possibilità alcuna al trapianto di cornea ed alla cecità. Una volta che il paziente torna con la diagnosi di cheratocono, la sua educazione (e quella della famiglia) è diventata una parte essenziale della gestione, al fine di consentire decisioni consapevoli e stabilire aspettative realistiche di trattamento.
A maggior ragione, pertanto, cerchiamo di inviare con celerità i casi più giovani (fino a 17 anni d’età) perché dai consensus italiani emerge l’indicazione ad eseguire tout court un CXL in questi soggetti, dato l’alto rischio di progressione, ma considerate che la topografia baseline è fondamentale per stabilire anche in soggetti più “anziani” una progressione (in genere ripetizione dell’esame entro 6 mesi) e quindi l’indicazione a CXL. I pazienti più giovani devono essere esaminati a intervalli di tempo più brevi.