La presbiopia è l’anomalia oculare in assoluto più diffusa (100% dei soggetti con più di 45 anni) ed è anche quella più invalidante in età lavorativa.
La compensazione o l’eliminazione della presbiopia è il Santo Graal della moderna oftalmologia.
Sappiamo che il diametro del cristallino cresce di circa 20 µm/anno e che man mano che il cristallino cresce si sposta in avanti, per cui anche l’inserzione delle fibre zonulari sul cristallino risulterà più anteriore (1, 2, 3, 4). Col tempo il cristallino diviene anche più rigido e più spesso nella sua porzione posteriore, mentre la curvatura della capsula anteriore si riduce (4).
Non è solo il cristallino a divenire meno deformabile, anche l’ora serrata perde progressivamente la sua capacità di spostarsi in avanti durante la fase accomodativa a causa della perdita di elasticità del corpo ciliare, della coroide e della sclera (5, 6, 7). In realtà, con il passare del tempo tutti i tessuti oculari perdono elasticità e divengono più rigidi (8) e nonostante il muscolo ciliare conservi la piena capacità di contrarsi (9) questo non è in grado di impedire la perdita completa della capacità accomodativa.
Questi elementi confermano l’ipotesi avanzata da Strenk (10) secondo cui la presbiopia è una patologia della disaccomodazione.
I dati sulla riduzione dell’ampiezza accomodativa in relazione all’età presentati da Duane nel 1912 (11) sono ancora usati come valori di riferimento. Come si può facilmente notare nella figura 1, la perdita di elasticità dei tessuti oculari inizia molto presto e già tra 12 e 25 anni vengono perse almeno 4D di ampiezza accomodativa. Non notiamo questa perdita solo perché non interferisce con le nostre necessità visive.

Tra 45 e 50 anni gli esseri umani avranno perso oltre 10 diottrie di ampiezza accomodativa, avranno una riserva accomodativa residua di circa 2 diottrie e questa condizione interferirà significativamente con le prestazioni visive per vicino, facendoci definire l’uomo presbite.
Soluzioni terapeutiche
Come abbiamo visto la presbiopia è determinata dalla somma di vari fattori e, anche per questo, non possediamo ancora un trattamento risolutivo ma vengono proposti innumerevoli approcci:
- gli occhiali multifocali rappresentano un valido sistema per la compensazione della presbiopia ma non sempre trovano una buona accettazione da parte dei presbiti, in particolare se questi non hanno mai portato correzioni ottiche in precedenza;
- la chirurgia propone innumerevoli tecniche (monovisione, mini-monovisione, cheratoplastica conduttiva, inserti corneali a foro stenopeico, inserti corneali a differente indice di rifrazione, inserti corneali ad aumento della profondità di fuoco, LASIK presbiopica periferica, LASIK presbiopica centrale, lenti intraoculari multifocali, lenti intraoculari accomodative, lenti intraoculari a profondità di fuoco estesa, impianti sclerali, ablazione sclerale laser) che possono dare un qualche grado d’indipendenza dagli occhiali per vicino ma richiedono l’accettazione irreversibile di rilevanti compromessi rispetto alla condizione visiva prima della presbiopia;
- le lenti a contatto rappresentano un approccio reversibile e sicuro alla compensazione della presbiopia.
Un aspetto che dev’essere tenuto in attenta considerazione poiché può ostacolare l’impiego delle lenti a contatto per la correzione della presbiopia è rappresentato dalla maggiore frequenza di occhio secco in età presbiopica soprattutto nella popolazione femminile. Per questa ragione le lenti a contatto morbide per la correzione della presbiopia propongono vari sistemi per attenuare la sintomatologia da occhio secco e rendere l’uso delle lenti più confortevole.

La figura 2 mostra le più comuni lenti a contatto per la correzione della presbiopia. Ciò che appare evidente è la stretta dipendenza del sistema di correzione dal diametro pupillare con le ben note conseguenze sulla qualità delle immagini: aloni, immagini fantasma, immagini che tendono a sdoppiarsi, perdita significativa di luminosità. In particolare quest’ultima rappresenta il problema più significativo che spesso induce all’abbandono della correzione con lenti a contatto multifocali. La quantità di luce che riesce a raggiungere la retina durante l’utilizzo di lenti a contatto multifocali raggiunge a malapena il 70%.

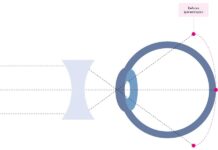
Oggi è disponibile una nuova categoria di lenti a contatto per la compensazione della presbiopia: le lenti a contatto afocali. Queste lenti (fig. 3) hanno il profilo di una normale lente sferica con al centro un bottone iper-rifrattivo di circa 1 mm che crea un’apparente estensione della profondità di campo. Questa strategia costruttiva libera la lente afocale dalla dipendenza dalla pupilla e, soprattutto, permette a più del 90% della luce di raggiungere la retina senza diffrazioni.

A differenza di tutte le altre lenti a contatto per la prebiopia, per le quali è necessario calcolare anche l’addizione, nel caso delle lenti afocali questo non è necessario, è sufficiente rilevare con precisione la migliore correzione ottica per lontano. Questo si traduce in una notevole riduzione dei tempi necessari all’individuazione della lente a contatto definitiva e in un processo di adattamento alla lente estremamente rapido da parte del paziente che - se è già un portatore di lenti a contatto - entro 15 minuti dall’applicazione è in grado di raggiungere i valori ottimali di visus sia per lontano sia per vicino.
Inoltre, la lente afocale è dotata di tecnologia “fusion” cioè è caricata con acido ialuronico e TSP che vengono rilasciati sulla superficie oculare garantendo un ottimo confort di utilizzo anche in soggetti con occhio secco.
Bibliografia
- Croft MA, McDonald JP, Katz A, Lin T-L, Lutjen-Drecoll E, Kaufman PL. Extralenticular and lenticular aspects of accommodation and presbyopia in human versus monkey eyes. Invest Ophthalmol Vis Sci 2013; 54:5035–5048.
- Croft MA, Nork TM, McDonald JP, Katz A, Lutjen-Drecoll E, Kaufman PL. Accommodative movements of the vitreous membrane, choroid, and sclera in young and presbyopic human and non human primate eyes. Invest Ophthalmol Vis Sci 2013; 54:5049–5058.
- Richdale K, Sinnott LT, Bullimore MA, Wassenaar PA, Schmalbrock P, Kao C-Y, Patz S, Mutti DO, Glasser A, Zadnik K. Quantification of age-related and per-diopter accommodative changes of the lens and ciliary muscle in the emmetropic human eye. Invest Ophthalmol Vis Sci 2013; 54:1095–1105.
- Werner L, Trindade F, Pereira F, Werner L. Physiology of accommodation and presbyopia. Arq Bras Oftalmol 2000; 63:503–509.
- Croft MA, Glasser A, Heatley G, McDonald JP, Ebbert T, Dahl DB, Nadkami NV, Kaufman PL. Accommodative ciliary body and lens function in rhesus monkeys, I: normal lens, zonule and ciliary process configuration in the iridectomized eye. Invest Ophthalmol Vis Sci 2006; 47:1076–1086.
- Stachs O, Martin H, Behrend D, Schmitz KP, Guthoff R. Three-dimensional ultrasound biomicroscopy, environmental and conventional scanning electron microscopy investigations of the human zonula ciliaris for numerical modeling of accommodation. Graefes Arch Clin Exp Ophthalmol 2006; 244:836-844
- Croft MA, McDonald JP, Nadkami NV, Lin T-L, Kaufman PL. Age-related changes in centripetal ciliary body movement relative to centripetal lens movement in monkey. Exp Eye Res 2009; 89:824-832
- Grossniklaus HE, Nickerson JM, Edelhauser HF, Bergman LAMK, Berglin L. Anatomic alterations in aging and age-related diseases of the eye. Invest Ophthalmol Vis Sci 2013; 54(14): ORSF23–ORSF27
- Sheppard AL, Davies LN. The effect of ageing on in vivo human ciliary muscle morphology and contractility. Invest Ophthalmol Vis Sci 2011; 52:1809–1816
- Strenk SA, Semmlow JL, Strenk LM, Munoz P, Gronlund-Jacob J,DeMarco JK. Age-related changes in human ciliary muscle and lens: a magnetic resonance imaging study. Invest Ophthalmol Vis Sci 1999; 40:1162–1169.
- Duane, A. Normal values of the accommodation at all ages. J. Am. Med. Assoc. 1912; 59:1010–1013
- Schiffman RM, Christianson MD, Jacobsen G, Hirsch JD, Reis BL. Reliability and validity of the Ocular Surface Disease Index. Arch Ophthalmol. 2000; 118:615-621