I picchi di pressione intraoculare (IOP) nell’immediato post-operatorio della chirurgia della cataratta rappresentano un evento frequente, spesso considerato transitorio e benigno. Tuttavia, nei pazienti a rischio – in particolare ipertesi oculari o glaucomatosi – anche aumenti pressori di breve durata possono avere conseguenze clinicamente rilevanti. Storicamente, gli ophthalmic viscosurgical devices (OVD) sono stati indicati come principali responsabili di questi picchi. Le evidenze disponibili suggeriscono invece un quadro più complesso, in cui la scelta dell’OVD è una variabile importante, ma non l’unica, e in cui la strategia chirurgica complessiva riveste un ruolo determinante (1,2).
IOP post-operatoria: inquadramento clinico e fisiopatologico
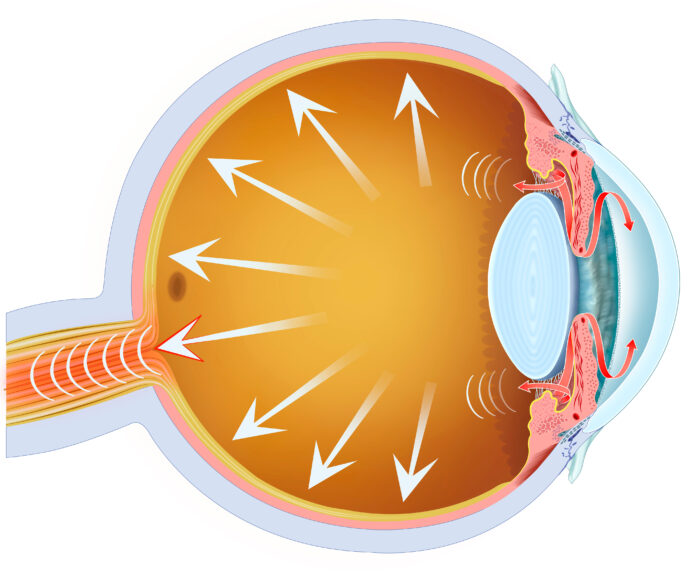
L’aumento dell’IOP dopo la facoemulsificazione si manifesta tipicamente nelle prime 4–24 ore dall’intervento e nella maggior parte dei casi è transitorio. La sua incidenza varia ampiamente nella letteratura, riflettendo differenze nella popolazione studiata, nella tecnica chirurgica e nei criteri di definizione del picco pressorio (3,4). Dal punto di vista fisiopatologico, il fenomeno è multifattoriale: contribuiscono l’ostruzione meccanica del trabecolato, l’infiammazione post-chirurgica, la presenza di detriti cellulari e, in modo rilevante, la ritenzione di OVD in camera anteriore o nello spazio retro-ottico (5).
OVD e aumento della IOP: evidenze e falsi miti
L’associazione tra OVD e ipertensione post-operatoria è ben documentata, ma spesso interpretata in modo riduttivo. Gli OVD non determinano un aumento pressorio di per sé; piuttosto, il problema nasce dalla loro ritenzione e dalla difficoltà di rimozione completa, che varia in funzione delle proprietà reologiche del prodotto impiegato (5,6). Studi comparativi hanno mostrato differenze nel comportamento pressorio tra OVD coesivi e dispersivi, ma nessuna classe può essere considerata intrinsecamente “pericolosa” in senso assoluto (3,4).
Gli OVD dispersivi, grazie alla loro maggiore adesività, tendono a persistere più a lungo sulle superfici intraoculari e nell’angolo irido-corneale, aumentando il rischio di ostruzione trabecolare se non rimossi adeguatamente. Gli OVD coesivi, al contrario, sono generalmente più facili da aspirare, ma possono rimanere intrappolati dietro l’IOL se la tecnica di wash-out non è ottimale (5,7).
Ritenzione dell’OVD e tecnica di rimozione
Le evidenze sperimentali e cliniche indicano che la ritenzione residua di OVD è il principale determinante dei picchi pressori post-operatori (5,8). Le aree critiche includono lo spazio retro-ottico e l’angolo camerulare, dove anche piccole quantità di viscoelastico possono interferire con il deflusso dell’umor acqueo. La probabilità di ritenzione è influenzata dalle proprietà di coesione e adesività dell’OVD, nonché dalla tecnica chirurgica, dalla fluidica utilizzata e dal tipo di IOL impiantata (6,7).
Studi in vitro e in vivo hanno dimostrato come OVD con bassa coesione e alta adesività richiedano manovre di aspirazione più meticolose, mentre OVD altamente coesivi possono essere rimossi in blocco, ma richiedono un’attenzione specifica allo spazio retro-capsulare (5,6).
Fattori chirurgici e pazienti a rischio
Il rischio di spike pressorio è amplificato da diversi fattori chirurgici, tra cui interventi prolungati, maggiore trauma tissutale e gestione subottimale della fluidica. Nei pazienti con glaucoma, anche aumenti pressori transitori possono tradursi in un peggioramento funzionale. In questi casi, la strategia sul migliore OVD da utilizzare assume un ruolo centrale e deve essere pianificata fin dalla fase preoperatoria (2,3).
Nella chirurgia combinata cataratta–glaucoma, il controllo dell’IOP post-operatoria è ancora più critico e la rimozione completa dell’OVD diventa una priorità assoluta per evitare interferenze con il deflusso o con le procedure filtranti (5,8).
La soluzione: un approccio OVD-tailored
Le evidenze cliniche indicano chiaramente che la prevenzione dei picchi pressori post-operatori non può basarsi esclusivamente sulla terapia farmacologica. Sebbene i farmaci ipotonizzanti possano essere utili in casi selezionati, la strategia più efficace rimane quella intraoperatoria. Un approccio realmente OVD-tailored prevede la scelta del viscoelastico in funzione del profilo di rischio pressorio del paziente, della fase chirurgica e della tecnica utilizzata, integrando in modo consapevole le proprietà reologiche del prodotto con le esigenze cliniche specifiche (1,2).
Nei pazienti a rischio elevato di ipertono post-operatorio, può essere appropriato privilegiare non solo OVD facilmente rimovibili o strategie combinate, ma anche l’impiego di OVD a coesività intermedia, caratterizzati da proprietà coesive sufficienti a consentire una gestione agevole dello spazio intraoculare e, al contempo, da una componente di comportamento dispersivo in grado di garantire una protezione endoteliale efficace. Dati clinici prospettici e randomizzati hanno dimostrato che alcuni OVD a base di ialuronato di sodio appartenenti a questa categoria non sono associati a incrementi clinicamente significativi della pressione intraoculare nel post-operatorio, anche in presenza di residui lasciati intenzionalmente in situ (9). Questa caratteristica rende gli OVD a coesività intermedia un’opzione particolarmente interessante nei casi in cui il controllo pressorio post-operatorio rappresenta una priorità, poiché consente di evitare manovre di irrigazione–aspirazione eccessivamente aggressive che potrebbero aumentare il rischio di danno endoteliale.
In tale contesto, tecniche mirate di aspirazione dietro la IOL, wash-out sequenziali e una gestione attenta della fluidica restano strumenti fondamentali, ma possono essere integrate in modo più flessibile grazie all’utilizzo di OVD con un profilo di sicurezza favorevole sul versante pressorio (5,7).
Evidenze cliniche a supporto della strategia
Studi randomizzati e meta-analisi hanno mostrato che le differenze assolute nella perdita endoteliale e nei picchi pressori tra i diversi OVD sono generalmente contenute nella popolazione generale, ma diventano clinicamente rilevanti nei pazienti a rischio (3,4). È inoltre emersa la non inferiorità clinica degli OVD a base di ialuronato di sodio di origine batterica rispetto a quelli di origine animale, sia in termini di protezione endoteliale sia di controllo pressorio, ampliando le opzioni disponibili senza compromessi in termini di sicurezza ed efficacia (8,9).
Bibliografia
- Kaur K, Gurnani B. Viscoelastics (ophthalmic viscosurgical devices). In: StatPearls. Treasure Island, FL: StatPearls Publishing; 2025.
- Borkenstein AF, Borkenstein EM, Malyugin B. Ophthalmic viscosurgical devices in challenging cases: a review. Ophthalmol Ther. 2021;10(4):831-843. doi:10.1007/s40123-021-00403-9
- Vajpayee RB, Verma K, Sinha R, Titiyal JS, Pandey RM, Sharma N. Comparative evaluation of efficacy and safety of ophthalmic viscosurgical devices in phacoemulsification. BMC Ophthalmol. 2005;5:17. doi:10.1186/1471-2415-5-17
- Van den Bruel A, Gailly J, Devriese S, Welton NJ, Shortt AJ, Vrijens F. The protective effect of ophthalmic viscosurgical devices on endothelial cell loss during cataract surgery: a meta-analysis using mixed treatment comparisons. Br J Ophthalmol. 2011;95(1):5-10. doi:10.1136/bjo.2009.158360
- Assia EI, Apple DJ, Lim ES, Morgan RC, Tsai JC. Removal of viscoelastic materials after experimental cataract surgery in vitro. J Cataract Refract Surg. 1992;18(1):3-9. doi:10.1016/S0886-3350(13)80002-9
- Poyer JF, Chan KY, Arshinoff SA. Quantitative method to determine the cohesion of viscoelastic agents by dynamic aspiration. J Cataract Refract Surg. 1998;24(8):1130-1135. doi:10.1016/S0886-3350(98)80149-7
- Higashide T, Sugiyama K. Use of viscoelastic substance in ophthalmic surgery—focus on sodium hyaluronate. Clin Ophthalmol. 2008;2(1):21-30.
- Daas L, Larrosa JM, Gavin A, Isanta C, Langenbucher A, Jackson BE, et al. Clinical comparison of the performance of two marketed ophthalmic viscosurgical devices: bacterially derived Healon PRO and animal-derived Healon. J Ophthalmol. 2020;2020:8874850. doi:10.1155/2020/8874850
- Pagnacco C, Tosi R, Dalsaso J, Fraccaroli S, Saggin F, Marchini G. A prospective, randomized, controlled clinical investigation comparing the efficacy and safety of sodium hyaluronate–based ophthalmic viscosurgical devices FIDIAL PLUS and IAL-F in cataract surgery. J Ocul Pharmacol Ther. 2024. doi:10.1089/jop.2024.0044