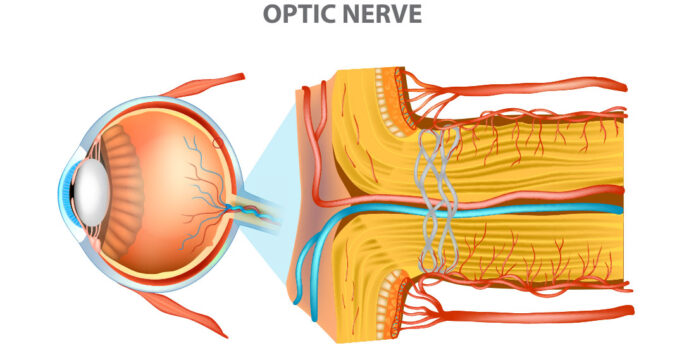
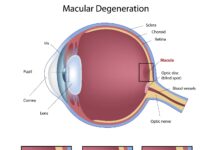
Nel panorama attuale della gestione del glaucoma, la neuroprotezione rappresenta un concetto ormai imprescindibile. Il glaucoma è infatti considerato una malattia neurodegenerativa che coinvolge l’intera via ottica, caratterizzata da una progressiva perdita delle cellule ganglionari retiniche e da un deterioramento funzionale che può progredire anche in presenza di un controllo pressorio apparentemente soddisfacente. Le recenti linee guida dell’European Glaucoma Society confermano questo cambio di paradigma, sottolineando come l’obiettivo terapeutico non possa limitarsi alla riduzione della pressione intraoculare, ma debba includere interventi complementari capaci di contrastare lo stress ossidativo, migliorare la funzione mitocondriale e preservare l’integrità anatomica e funzionale del sistema visivo nel lungo periodo (1).
Basi biologiche della neuroprotezione
Il razionale biologico della neuroprotezione poggia su diversi meccanismi patogenetici che concorrono alla morte delle cellule ganglionari. Le evidenze raccolte mostrano come la disfunzione mitocondriale, la neuroinfiammazione e la riduzione dei fattori trofici svolgano un ruolo determinante nella progressione del danno glaucomatoso. La citicolina e la nicotinamide emergono come due delle molecole più promettenti, grazie alla loro capacità di intervenire su processi fondamentali della bioenergetica neuronale. In particolare, la citicolina contribuisce al mantenimento dei fosfolipidi di membrana e della funzione mitocondriale, modulando anche i livelli di neurotrasmettitori come dopamina, acetilcolina e noradrenalina, elementi cruciali per il corretto funzionamento retinico e corticale. La nicotinamide agisce come precursore essenziale del NAD⁺, una molecola chiave per il metabolismo energetico e la sopravvivenza neuronale, sostenendo l’attività mitocondriale, contrastando lo stress ossidativo e favorendo la resilienza delle cellule ganglionari retiniche (2).
Evidenze precliniche: l’asse citicolina–nicotinammide
La ricerca preclinica fornisce un supporto solido alla neuroprotezione. Nel modello murino di glaucoma ipertensivo studiato da Melecchi et al., la combinazione di nicotinamide e citicolina ha mostrato un beneficio rilevante, capace di salvaguardare circa la metà delle cellule ganglionari che altrimenti sarebbero andate incontro ad apoptosi. Questo recupero biologico si traduce anche in un significativo miglioramento della risposta elettroretinografica, con una marcata riduzione dei marker di stress ossidativo e di infiammazione. Tale osservazione apre prospettive interessanti sulla possibilità di adottare combinazioni terapeutiche mirate a differenti livelli della cascata patologica glaucomatosa (3).
Aspetti regolatori e sicurezza delle molecole neuroprotettive
Anche le normative europee e nazionali vanno tenute in considerazione. La citicolina è riconosciuta come “nuovo alimento” e la sua commercializzazione segue un preciso iter regolatorio stabilito dal Regolamento UE del 2018, che ne definisce i requisiti di sicurezza e composizione (4). Parallelamente, il Ministero della Salute italiano stabilisce i limiti di apporto massimo consentiti per le vitamine nei supplementi, fissando per la niacina un limite di 54 mg al giorno per la popolazione adulta, un dato utile per orientare la prescrizione e prevenire l’assunzione eccessiva in associazione con altri prodotti nutrizionali (5). Il profilo delle diverse forme chimiche di niacina è ulteriormente approfondito nella revisione di MacKay, che discute le differenze di biodisponibilità e sicurezza tra nicotinammide, nicotinic acid, esteri e forme a rilascio prolungato, informazioni rilevanti soprattutto quando il clinico si trova a valutare prodotti a composizione complessa (6).
Marker fisiologici e metabolici emergenti
Nell’ambito della fisiologia retinica, strumenti come il pattern electroretinogram e la fotopic negative response stanno assumendo un’importanza crescente grazie alla loro capacità di intercettare precocemente disfunzioni delle cellule ganglionari, spesso prima che si manifestino alterazioni perimetriche o strutturali.
Parallelamente, anche la valutazione di metaboliti coinvolti nella funzione mitocondriale sta guadagnando spazio e si collega direttamente all’interesse per la nicotinammide. Tuttavia, l’impiego di questa molecola e dei suoi derivati richiede prudenza: studi condotti in ambito cardiovascolare, come quello di Ferrell e colleghi, hanno evidenziato come i metaboliti terminali in eccesso, in particolare 2PY e 4PY, siano associati a un incremento del rischio di eventi cardiovascolari tramite l’induzione di mediatori infiammatori endoteliali. Pur non essendo un dato specifico per la popolazione glaucomatosa, esso suggerisce che la valutazione della sicurezza e delle dosi rivesta un ruolo essenziale quando si considerano supplementi nutrizionali per la neuroprotezione (7).
Aderenza terapeutica e prospettive farmacotecniche
La questione dell’aderenza terapeutica, fondamentale in una malattia cronica come il glaucoma, trova spunti interessanti anche in settori farmacologici apparentemente lontani dall’oftalmologia. Le analisi sull’uso delle compresse masticabili evidenziano come tali formulazioni migliorino la compliance nei pazienti con difficoltà di deglutizione, una condizione non infrequente anche in età avanzata, fascia in cui il glaucoma è maggiormente prevalente (8). Sebbene il tema riguardi principalmente farmaci sistemici, l’osservazione fornisce indicazioni potenzialmente utili per lo sviluppo futuro di integratori neuroprotettivi con migliori caratteristiche di tollerabilità e facilità d’uso. Le compresse masticabili consentono di ottenere un dosaggio preciso e standardizzato, spesso più affidabile rispetto alle formulazioni liquide, che possono essere soggette a variabilità nella misurazione e nella stabilità del principio attivo. Oltre al vantaggio farmacotecnico, queste formulazioni favoriscono l’aderenza terapeutica grazie a una migliore deglutibilità e alla possibilità di rispondere a esigenze specifiche dei pazienti, incluse preferenze dietetiche o intolleranze alimentari, come prodotti senza componenti di origine animale, privi di zuccheri, lattosio o glutine. Inoltre, aspetti pratici come la facilità di conservazione, la stabilità a temperatura ambiente e la praticità durante il trasporto contribuiscono in modo significativo al mantenimento della terapia. È plausibile immaginare, in un futuro non troppo lontano, lo sviluppo di compresse masticabili pensate appositamente per integrare molecole neuroprotettive, ottimizzando così l’accettabilità e l’aderenza tra i pazienti glaucomatosi (9).
Bibliografia
- European Glaucoma Society. Terminology and Guidelines for Glaucoma. 5th ed. 2020.
- D’Angelo A, et al. J Clin Med. 2024;13:2214.
- Melecchi A, et al. Front Med. 2023;10:1230941.
- Commissione Europea. Regolamento di esecuzione (UE) 2018/1023. 2018.
- Ministero della Salute. Apporti giornalieri di vitamine e minerali ammessi negli integratori alimentari. Revisione 2021.
- MacKay D, et al. Nutr Rev. 2012;70(6):357-366.
- Ferrell N, et al. Nat Med. 2024
- Antil A, et al. Syst Rev Pharm. 2023;14(9):571-577.
- Subramanian M, et al. IntechOpen; 2023.