Le lacrime non sono soltanto il modo più immediato con cui esprimiamo emozioni o proteggiamo la superficie oculare: sono anche una matrice biologica ricca di informazioni, capace di riflettere processi infiammatori, immunitari e neuro-sensoriali utili per la diagnosi, la stratificazione e il monitoraggio di molte condizioni oculari.
Durante l’European Vision and Eye Research (EVER) Meeting svoltosi a Firenze, la sessione “Tear Fluid Biomarkers of the Ocular Surface” ha riunito esperti internazionali nello studio delle lacrime e della superficie oculare.
Organizzato dalle dr.sse Marlies Gijs e Amalia Enríquez-de-Salamanca, con la moderazione della prof.ssa Piera Versura, l’incontro ha proposto un percorso che unisce ricerca avanzata e potenziali ricadute pratiche per il clinico, dalla qualità del campione alla lettura biologica dei sintomi. Nello specifico, sono stati presentati gli sviluppi più recenti nella ricerca sui biomarcatori lacrimali, con focus su metodologia di raccolta, standardizzazione dei protocolli, immunologia della superficie oculare e applicazioni nel dry eye disease. Gli interventi hanno inoltre esplorato il valore dei marker lacrimali nello studio del dolore oculare e nella definizione di fenotipi clinico-biologici, evidenziando il potenziale delle analisi multi-omics e dei futuri dispositivi point-of-care. Nel complesso, la sessione ha confermato le lacrime come “laboratorio” accessibile e ripetibile, promuovendo un percorso verso la medicina di precisione e rafforzando il ruolo di EVER come piattaforma di riferimento, in vista del congresso 2026 che tornerà a Firenze.
Perché cercare biomarcatori nel dry eye disease
Il prof. Christophe Baudouin ha ricordato come la malattia dell’occhio secco rappresenti una delle condizioni più invalidanti della superficie oculare, non solo per la sua diffusione ma per l’impatto significativo sulla qualità di vita dei pazienti. Il dry eye non può essere ridotto a una semplice carenza quantitativa di lacrime correggibile con la lubrificazione: è piuttosto una alterazione funzionale e anatomica della barriera di superficie, fondamentale per proteggere l’occhio da un ambiente potenzialmente aggressivo.
Il film lacrimale, costantemente esposto a stimoli ambientali difficilmente controllabili, contribuisce inoltre alla qualità visiva, rappresentando la prima interfaccia attraversata dalla luce prima di raggiungere la retina. Ne deriva che il discomfort visivo e i sintomi riferiti dal paziente sono il risultato combinato di una quantità insufficiente e, soprattutto, di una qualità inadeguata del film lacrimale.
Il dry eye è una condizione multifattoriale, sostenuta da cause spesso concomitanti: disordini ormonali e cutanei, malattie autoimmuni, tossicità iatrogena da farmaci o colliri, chirurgia refrattiva o della cataratta, uso prolungato di lenti a contatto. Questi fattori concorrono a instaurare un circolo vizioso in cui instabilità del film lacrimale e iperosmolarità determinano attrito meccanico, stimolazione delle terminazioni nervose corneali e attivazione di risposte infiammatorie che, a loro volta, peggiorano ulteriormente la qualità delle lacrime.
Un ruolo rilevante è svolto anche dalla disfunzione delle ghiandole di Meibomio: le alterazioni qualitative dei lipidi favoriscono evaporazione e instabilità del film lacrimale, creando un microambiente che facilita proliferazione microbica e infiammazione locale. A ciò si aggiunge l’impatto dei fattori ambientali – inquinanti atmosferici, particolato fine, gas irritanti, ozono e allergeni – che contribuiscono alle forme di “dry eye ambientale” (fig. 1).
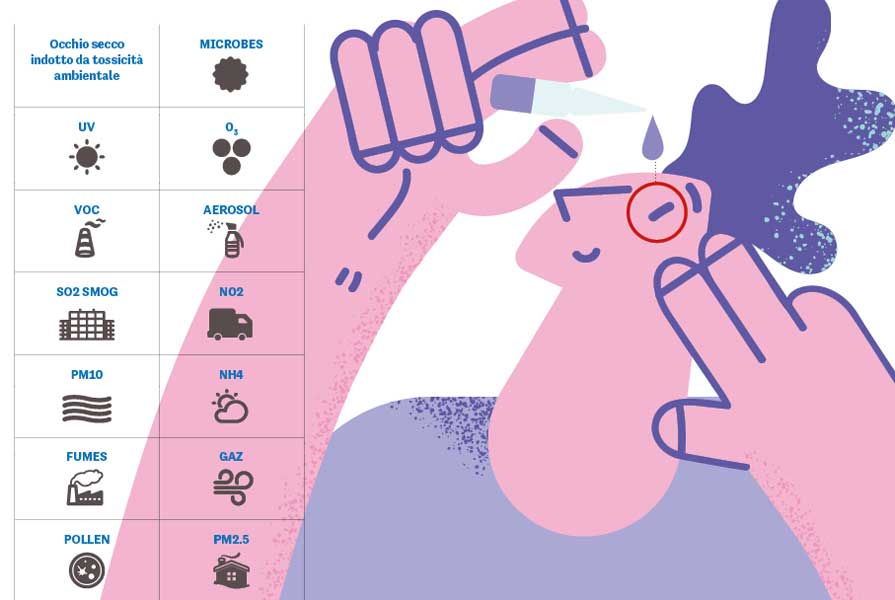
In questo contesto complesso, il prof. Baudouin ha evidenziato come i biomarcatori lacrimali rappresentino uno strumento essenziale per misurare i meccanismi biologici predominanti nel singolo paziente: infiammazione, stress ossidativo, componenti allergiche, microbiche, tossiche o ambientali. Le analisi omiche del film lacrimale hanno già identificato centinaia di proteine coinvolte in difesa immunitaria, metabolismo, risposta allo stress e integrità strutturale, ampliando la comprensione della malattia anche attraverso lipidomica, metabolomica e microbiomica.
Sebbene la sessione abbia posto l’accento su biomarcatori emergenti e approcci multi-omici, l’esperienza clinica ricorda che marker già validati, come HLA-DR, hanno aperto la strada all’utilizzo delle lacrime e della superficie oculare come strumenti di valutazione dell’attivazione infiammatoria. La sfida traslazionale resta la selezione di pannelli ristretti di biomarcatori robusti, validabili in modo riproducibile e utilizzabili con test semplici, idealmente utilizzando tecnologie point-of-care. Come sottolineato dal prof. Baudouin, la ricerca sui biomarcatori non è fine a sé stessa: per ottenere risposte clinicamente utili è necessario porre le domande giuste, identificando quali meccanismi guidano la malattia nel singolo paziente e come questi possano orientare una terapia realmente personalizzata (inbox 1).

Dalla raccolta al dato: ottimizzare il campione per le analisi multi-omics
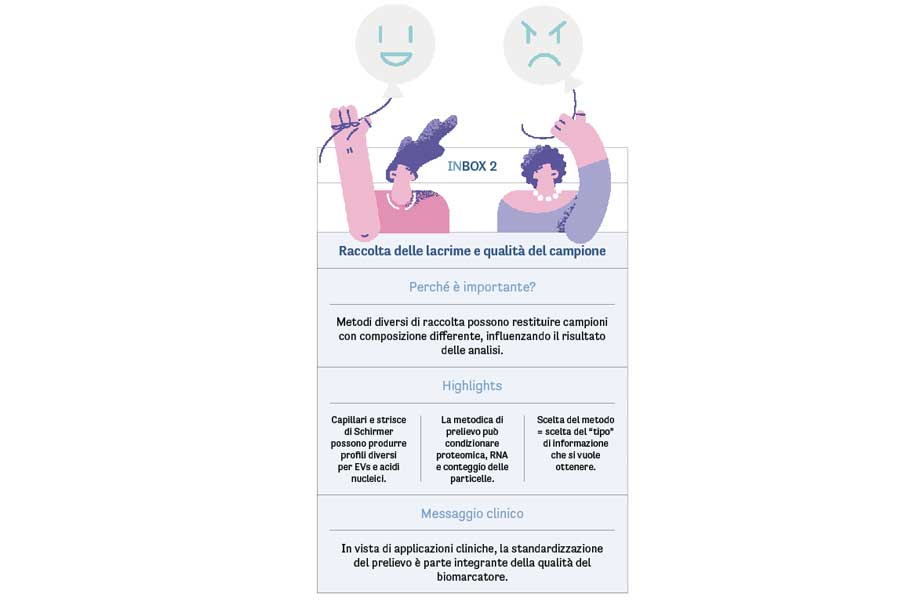
La raccolta del film lacrimale è uno dei passaggi più critici per trasformare le lacrime in uno strumento informativo utile. Capillari, microspugne e strisce di Schirmer non producono campioni equivalenti: variano per volume, composizione e per il tipo di molecole che preservano o trattengono. In questo contesto, la dr.ssa Clemence Bonnet ha mostrato come la scelta del metodo di prelievo condizioni in modo sostanziale la resa delle analisi multi-omics. Nel confronto tra capillari e strisce di Schirmer, i profili proteomici risultano in parte sovrapponibili, ma emergono differenze rilevanti nel recupero di vescicole extracellulari (EVs) e di acidi nucleici: le strisce possono trattenere una quota maggiore di EVs nel supporto, influenzando il conteggio delle particelle e la quantità di RNA disponibile. Anche i progetti dedicati al “viroma lacrimale” confermano che la metodica di raccolta può modificare sensibilmente ciò che viene misurato.
Il messaggio per i clinici è diretto: la fase preanalitica non è un dettaglio, ma un determinante dell’interpretazione. Affinché le lacrime possano supportare decisioni cliniche (diagnosi, follow-up, valutazioni preoperatorie), è essenziale adottare protocolli coerenti con l’obiettivo biologico e con la tecnologia utilizzata (inbox 2).
Standardizzare per rendere confrontabili gli studi
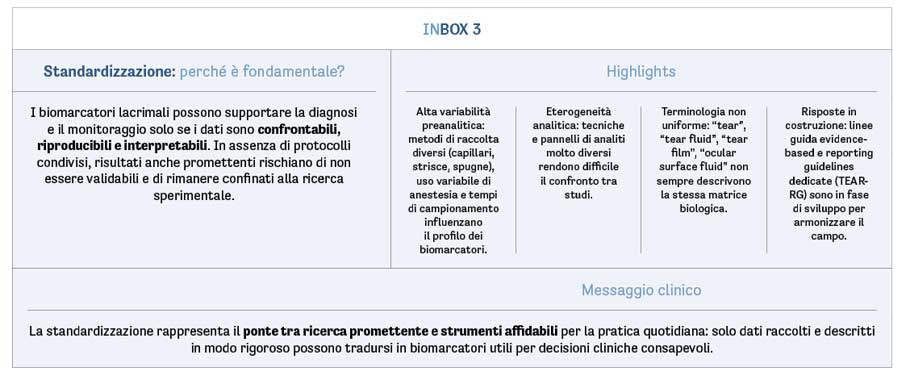
La dr.ssa Marlies Gijs ha affrontato una delle principali barriere alla reale traslazione clinica dei biomarcatori lacrimali: la mancanza di standardizzazione. I dati presentati mostrano come la ricerca in questo ambito sia in forte crescita, con un aumento costante delle pubblicazioni negli ultimi anni; tuttavia, questa espansione quantitativa non è stata accompagnata da un’adeguata armonizzazione dei protocolli. Il risultato è un’elevata eterogeneità metodologica che rende difficile confrontare gli studi, aggregare le evidenze e trarre conclusioni solide.
Le differenze riguardano l’intera filiera della ricerca: modalità di raccolta (capillari, strisce di Schirmer, spugne, lavaggi della superficie oculare), tipo di lacrime analizzate (basali, riflesse, stimolate), uso o meno di anestesia, tempi di campionamento, gestione del campione e tecniche analitiche impiegate. Anche il numero e il tipo di analiti studiati variano in modo marcato, passando da singoli marker a pannelli molto estesi, con metodiche che spaziano dall’immunodosaggio alla proteomica e alle altre tecnologie omiche.
Un ulteriore elemento critico è rappresentato dalla terminologia. Termini come “tear”, “tear fluid”, “tear film” e “ocular surface fluid” vengono spesso utilizzati come sinonimi, ma non sempre descrivono in modo univoco la matrice biologica analizzata o la procedura di raccolta. Questa ambiguità semantica, emersa chiaramente dalla revisione della letteratura, contribuisce a ridurre la riproducibilità degli studi e a ostacolare il confronto tra risultati provenienti da gruppi diversi.
Per rispondere a queste criticità, la dr.ssa Gijs ha illustrato il ruolo del Tear Research Network (tearresearchnetwork.com/), un’iniziativa internazionale che riunisce ricercatori e clinici con l’obiettivo di costruire un linguaggio comune e protocolli condivisi. Le attività del network includono lo sviluppo di linee guida evidence-based per la raccolta e l’analisi delle lacrime e la definizione di reporting guidelines dedicate (TEAR-RG), pensate per garantire descrizioni metodologiche complete, trasparenti e replicabili.
Il messaggio per il clinico è chiaro: senza standardizzazione, anche il biomarcatore più promettente rischia di rimanere confinato alla ricerca sperimentale. La futura “clinica dei biomarcatori lacrimali” dipenderà dalla solidità metodologica costruita oggi, condizione indispensabile per trasformare dati complessi in strumenti affidabili e utili nella pratica quotidiana (inbox 3).
Immunità oculare, infiammazione e scenari traslazionali
La dr.ssa Alessandra Micera ha descritto le lacrime come una matrice biologica “attiva”, capace di integrare segnali immunitari, neuro-sensoriali e metabolici. Oltre ai componenti classici (elettroliti, immunoglobuline, enzimi antimicrobici, lipidi e mucine), le lacrime contengono citochine e chemochine, fattori di crescita, neuromediatori, ormoni e metaboliti che possono riflettere condizioni locali e sistemiche.
Un punto centrale dell’intervento è stato il ruolo dell’infiammazione: profili di citochine (ad esempio IL-1β, IL-6, IL-8, TNF-α) e marker di danno di barriera (come MMP-9) possono indicare lo sbilanciamento tra risposte pro-infiammatorie e regolatorie, aiutando il clinico nella fenotipizzazione del dry eye (da deficit acquoso vs evaporativo) e nel monitoraggio della risposta a terapie antinfiammatorie o immunomodulanti. È stato inoltre richiamato il concetto di inflammaging: una parainfiammazione legata all’età che può contribuire a cronicizzazione dei sintomi e fallimenti clinici, soprattutto in contesti peri-operatori.
La dr.ssa Micera ha esteso la prospettiva a scenari interdisciplinari, inclusa l’oncologia: specifiche molecole infiammatorie, fattori angiogenici (es. VEGF) e neuropeptidi possono riflettere stati sistemici e condizioni associate a patologie neoplastiche, aprendo alla possibilità di usare le lacrime per screening/triage e monitoraggio in pazienti con coinvolgimento oculare o in terapia. La direzione futura punta a integrare fenotipizzazione clinica, strumenti strumentali e analisi multi-omics, con soluzioni point-of-care e lab-on-chip supportate da AI (inbox 4).

Dolore oculare e biomarcatori lacrimali: oltre la discrepanza tra segni e sintomi
Nel suo intervento, la dr.ssa Amalia Enríquez-de-Salamanca ha affrontato in modo approfondito il tema del dolore oculare, uno dei sintomi più complessi e frustranti nella gestione delle patologie della superficie oculare. Spesso il dolore riferito dal paziente risulta sproporzionato rispetto ai segni clinici osservabili, oppure persiste nonostante un apparente controllo della malattia di base. Questo scollamento tra sintomi e segni suggerisce l’esistenza di meccanismi biologici più articolati, che vanno oltre la semplice infiammazione superficiale.
La relatrice ha sottolineato come il dolore oculare possa derivare da componenti diverse — nocicettive, infiammatorie e neuropatiche — che spesso coesistono nello stesso paziente. In questo contesto, le lacrime rappresentano una matrice biologica particolarmente informativa, poiché riflettono in modo diretto l’attività delle fibre nervose corneali, lo stato infiammatorio locale e l’interazione tra sistema nervoso e sistema immunitario.
Attraverso l’analisi dei biomarcatori lacrimali è possibile identificare firme molecolari associate alla sensibilizzazione periferica e centrale. Citochine pro-infiammatorie, chemochine e mediatori lipidici indicano l’attivazione di processi infiammatori persistenti, mentre neuropeptidi e fattori neurotrofici — come NGF e BDNF — riflettono alterazioni della funzione nervosa e del dialogo neuro-immune. Questi segnali biologici aiutano a spiegare perché alcuni pazienti sviluppino dolore cronico anche in presenza di segni clinici minimi.
Un aspetto di particolare interesse riguarda il valore predittivo dei biomarcatori lacrimali. La dr.ssa Enríquez-de-Salamanca ha mostrato come specifici profili molecolari possano essere associati a un aumentato rischio di dolore persistente in contesti quali il post-operatorio o le patologie croniche della superficie oculare. Questo apre alla possibilità di identificare precocemente i pazienti a rischio e di adottare strategie preventive o terapeutiche mirate.
Il messaggio clinico finale è di grande rilevanza: il dolore oculare non dovrebbe più essere considerato solo come un sintomo soggettivo, ma come l’espressione di meccanismi biologici misurabili. L’integrazione dei biomarcatori lacrimali con la valutazione clinica tradizionale consente una migliore stratificazione dei pazienti, orienta la scelta terapeutica — antinfiammatoria, neuromodulante o combinata — e rappresenta un passo concreto verso una gestione più personalizzata e consapevole del dolore oculare (inbox 5).

Conclusioni
La sessione ha ribadito con forza che le lacrime possono evolvere da semplice fluido biologico a strumento clinico concreto solo attraverso l’integrazione di tre livelli fondamentali: la qualità del campione, la standardizzazione dei protocolli e la validazione traslazionale dei biomarcatori in contesti clinici reali. Senza questi passaggi, il potenziale informativo delle lacrime rischia di rimanere confinato alla ricerca sperimentale.
In questo scenario, diventa centrale il ruolo del clinico: conoscere le possibilità offerte dalla ricerca sui biomarcatori lacrimali significa acquisire nuovi strumenti interpretativi per leggere la complessità della superficie oculare. Non si tratta di sostituire l’esame clinico tradizionale, ma di iniziare a interrogarsi se e quando l’informazione biologica contenuta nelle lacrime possa rispondere a un bisogno clinico reale, migliorando la qualità delle decisioni diagnostiche e terapeutiche, soprattutto nei casi più complessi o refrattari.
La ricerca sta infatti superando l’approccio basato sul singolo biomarcatore per orientarsi verso cluster molecolari robusti, capaci di definire fenotipi biologici specifici della superficie oculare. Questo passaggio apre la strada a una stratificazione più precisa dei pazienti, a una migliore previsione della risposta terapeutica e a un monitoraggio più mirato nel tempo, in linea con i principi della medicina di precisione.
EVER 2025 ha confermato il ruolo delle lacrime come ponte tra ricerca di base e pratica clinica. L’appuntamento è ora rinnovato ancora a Firenze per EVER 2026 (15-17 ottobre), dove questo percorso verso una medicina della superficie oculare sempre più predittiva, personalizzata e integrata proseguirà con nuove evidenze scientifiche e tecnologie emergenti.