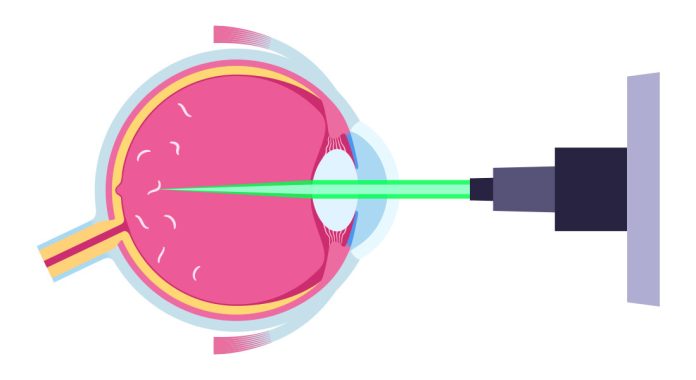
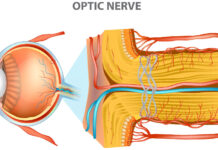
La gestione dei corpi mobili vitreali rappresenta un tema di grande interesse nella pratica vitreoretinica, grazie ai progressi nella comprensione della fisiopatologia del vitreo e all’evoluzione delle tecniche chirurgiche. Il vitreo, pur essendo costituito quasi interamente da acqua, è una matrice extracellulare finemente organizzata in cui collagene e acido ialuronico cooperano per mantenere trasparenza, viscoelasticità e funzione biomeccanica. Con l’avanzare dell’età, questa struttura si degrada progressivamente: l’acido ialuronico perde coesione con le fibrille collagene, le quali tendono ad aggregarsi e determinando sineresi e miodesopsie. Tale processo degenerativo è amplificato da un aumento delle specie reattive dell’ossigeno e da una diminuzione delle difese antiossidanti, contribuendo alla degradazione del gel vitreale e alla formazione di opacità persistenti [1].
Il distacco posteriore del vitreo (PVD) rappresenta un momento cruciale nell’evoluzione delle miodesopsie. Quando la corticale vitreale posteriore si separa dalla retina, il gel collassa verso la regione centrale della cavità vitreale, rendendo più evidente la percezione delle opacità. In molti casi, il fenomeno è autolimitante, ma una percentuale significativa di pazienti continua a percepire disturbi visivi rilevanti, tanto maggiori quanto le opacità sono vicine alla retina. È in questo contesto che si inserisce il concetto di Vision Degrading Myodesopsia (VDM), una condizione patologica in cui la persistente (6-12 mesi) percezione soggettiva delle opacità durante tutte le attività quotidiane si associa a uno stato di ansia e stress. Il VDM si associa anche ad un peggioramento oggettivo della sensibilità al contrasto e dello straylight, in presenza di un’acuità visiva conservata. Vari strumenti diagnostici, come l’ecografia B scan e la modellizzazione ottica, permettono oggi una correlazione più precisa tra morfologia delle opacità e impatto funzionale, migliorando la selezione dei candidati al trattamento [2].
Approccio conservativo e limiti della vitreolisi YAG
Il trattamento conservativo è spesso la prima scelta, soprattutto nei casi recenti o in corso di PVD acuto. La vitreolisi YAG laser è stata proposta come opzione minimamente invasiva, ma la sua efficacia rimane oggetto di discussione. Molti pazienti non riportano un beneficio significativo e studi prospettici randomizzati non dimostrano risultati superiori al placebo. Inoltre, la gestione delle opacità mobili con YAG pone rischi specifici, tra cui il potenziale danno del cristallino o la possibilità di indurre rotture retiniche iatrogene [2].
Vitrectomia pars plana: il trattamento più efficace nei casi selezionati
La vitrectomia pars plana è oggi considerata l’unico approccio efficace per i pazienti con VDM severa e refrattaria. L’introduzione di strumenti sutureless e di piccolo calibro, come 25G e 27G, ha ridotto l’invasività della procedura, facilitando il recupero postoperatorio e migliorando globalmente il profilo di sicurezza. I risultati clinici evidenziano un’alta soddisfazione dei pazienti e un miglioramento significativo della qualità visiva. Un tema molto discusso riguarda la scelta tra la vitrectomia completa e quella “limited”. Quest’ultima, evitando l’induzione del PVD, riduce il rischio di complicanze intraoperatorie quali la cataratta e il distacco di retina, pur garantendo buoni risultati anatomico funzionali [3,4].
Complicanze e gestione postoperatoria
Tra le complicanze della vitrectomia, la cataratta rappresenta la più frequente nei pazienti fachici, con incidenza variabile in rapporto alle tecniche adottate e al calibro degli strumenti. Rotture retiniche e distacco di retina, pur essendo complicanze potenzialmente gravi, risultano relativamente rare quando l’intervento è eseguito da chirurghi esperti e preceduto da un’accurata selezione preoperatoria. In questo contesto, l’impiego di coloranti del vitreo, come il triamcinolone acetonide, consente una migliore visualizzazione delle strutture vitreali e della corticale posteriore, facilitandone la rimozione completa e riducendo il rischio di complicanze intraoperatorie. In alcuni pazienti, il distacco posteriore di vitreo non indotto durante l’intervento può manifestarsi successivamente e determinare la ricomparsa di miodesopsie e di eventuali rotture retiniche; tali evenienze possono tuttavia essere gestite efficacemente mediante un nuovo intervento [4].
Fattori sistemici e influenza dell’idratazione sulla biologia vitreale
La ricerca recente ha iniziato a esplorare anche fattori sistemici che potrebbero influenzare la biologia del vitreo. La struttura del gel vitreale, fortemente dipendente dai suoi equilibri idrici e osmotici, potrebbe teoricamente essere sensibile a variazioni dello stato di idratazione dell’organismo. Studi fisiologici suggeriscono che squilibri idroelettrolitici o condizioni di ipovolemia possano modulare processi infiammatori oculari o influenzare la diffusione dei soluti nei fluidi intraoculari. Il possibile ruolo del sistema renina–angiotensina–aldosterone nella regolazione oculare rappresenta un ulteriore elemento di interesse, indicando un potenziale legame tra idratazione, stress ossidativo e alterazioni vitreali. Futuri studi specifici per validare quest’ipotesi saranno necessari [5].
Bibliografia
- Sebag J. Vitreous and vision degrading myodesopsia. Prog Retin Eye Res. 2020;79:100847.
- Ankamah E, Sebag J, Ng E, et al. Vitreous floaters: Diagnosis and management. Surv Ophthalmol. 2020;65(5):560-580.
- Broadhead GK, Hong T, Zhu M, et al. Outcomes of pars plana vitrectomy for visually significant vitreous opacities. Clin Exp Ophthalmol. 2022;50(2):123-131.
- Sebag J, Yee KM, Nguyen JH, et al. Office-based limited vitrectomy for vision degrading myodesopsia. Retina. 2022;42(7):1325-1335.
- Sherwin JC, Kokavec J, Thornton SN. Hydration, fluid regulation and the eye: In health and disease. Clin Exp Ophthalmol. 2015;43(8):749-764.
- Sprott H, Fleck C. Hyaluronic acid in rheumatology. 2023;15(9):2247.