La cheratoplastica lamellare anteriore profonda (DALK) sta progressivamente soppiantando la cheratoplastica a tutto spessore nel trattamento chirurgico delle alterazioni di forma e trasparenza della cornea per le patologie corneali stromali in presenza di un endotelio sano. La tecnica della Big-Bubble DALK di seguito descritta nei dettagli della procedura chirurgica rappresenta oggi la tecnica più comunemente impiegata.
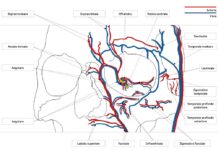
La cheratoplastica lamellare anteriore prevede la sostituzione eterotopica lamellare degli strati anteriori della cornea mantenendo gli strati posteriori della cornea ricevente, specificamente la membrana di Descemet (DM) e lo strato endoteliale. Lo svantaggio principale della cheratoplastica lamellare anteriore rispetto alla cheratoplastica penetrante (PK) è il rischio di sviluppo di irregolarità del letto stromale del ricevente che può verificarsi dopo una dissezione lamellare manuale, con potenziale limitazione dell'acuità visiva finale. Per ovviare a questo problema sono stati ideati diversi approcci, tra cui l'utilizzo di un microcheratomo (1-2) per ottenere una dissezione stromale regolare o l'escissione manuale dello stroma malato fino all’esposizione della membrana di Descemet (DM) (3). Sono state descritte diverse tecniche chirurgiche per l'esecuzione della DALK "a massima profondità", in cui si esegue la rimozione completa dello stroma con l'esposizione della DM nell'asse visivo centrale (3-8). Queste tecniche includono l'uso di materiali viscoelastici (9-10), fluidi o aria iniettati nello stroma profondo per facilitare la separazione dello stroma profondo dalla DM (3) (figura 1).
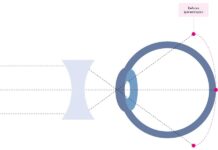
La tecnica "Big-Bubble" di Anwar per la cheratoplastica lamellare anteriore profonda (DALK) consiste nella separazione della membrana di Descemet unitamente ad un sottile strato stromale pre-descemetico (pre-DM), recentemente definito come strato pre-DM o strato di Dua, mediante l'iniezione forzata di aria nello stroma profondo mediante ago o cannula inseriti nello stroma profondo (4) (figura 2).

Per ottenere con successo la separazione della pre-DM dallo stroma posteriore, l'ago o la cannula devono essere posizionati in prossimità della DM, in modo che l'aria possa raggiungere il punto corretto per il clivaggio degli strati (11-12). Questa tecnica ha una difficile curva di apprendimento ed è controindicata in alcune patologie in cui la DM può essere interrotta o coinvolta in esiti cicatriziali stromali profondi (3). Il successo della separazione della pre-DM con la tecnica Big-Bubble è stato riportato avvenire nel 60-70% dei casi con l'utilizzo di un ago (30 o 27 Gauge) e nell'80-90% dei casi con l'impiego di una cannula dedicata con punta smussata per l'iniezione di aria (13-14).
La tecnica Big-Bubble per la DALK consente di ottenere buoni risultati visivi soprattutto nei pazienti affetti da cheratocono. Ciò è essenzialmente dovuto alla formazione di un'interfaccia regolare tra donatore e ricevente che si realizza tra lo strato pre-DM e lo stroma del donatore, riducendo al minimo le irregolarità dell'interfaccia donatore-ricevente. Il passo più critico per ottenere con successo la formazione della bolla rimane l'inserimento dell'ago o della cannula nello stroma: una posizione troppo superficiale dello strumento di solito provoca un enfisema corneale diffuso senza formazione della bolla, mentre un inserimento troppo profondo può portare alla perforazione intraoperatoria accidentale della DM, richiedendo la conversione in PK, in alcuni casi (15). Sono state proposte diverse tecniche per valutare la profondità intrastromale, tra cui l'aria o il triamcinolone iniettati in camera anteriore, l’impiego di una lampada a fessura accoppiata a un microscopio chirurgico e, recentemente, la tomografia a coerenza ottica del segmento anteriore (AS-OCT) intraoperatoria combinata con la tecnologia del laser a femtosecondi per guidare l'inserimento della cannula vicino al piano della DM (11,16-17). Nei casi in cui non si dovesse ottenere il clivaggio mediante la tecnica Big-Bubble, la DALK può comunque essere eseguita mediante dissezione manuale. La DALK con dissezione manuale può anche essere considerata la procedura di scelta nelle cicatrici corneali a tutto spessore o nei casi in cui la DM è patologica, come nelle perforazioni corneali, nell'idrope corneale pregressa o negli esiti di cheratotomia radiale (3).
Tecnica chirurgica
Poco prima dell'intervento, alcune gocce di tropicamide 1% (Visumidriatic 1%; Visufarma Spa, Italia) vengono instillate nel fornice inferiore per ottenere la midriasi. La dilatazione della pupilla determina un riflesso rosso vivo, utile per la centratura del trapano e la localizzazione di un piano stromale profondo per l'iniezione di aria. Dopo aver marcato il centro geometrico della cornea, si esegue una trapanazione circolare a spessore parziale del diametro desiderato (generalmente 8-9 mm) fino all'80% dello spessore corneale, utilizzando un trapano a suzione a profondità regolabile (One step Moria, Antony, Francia). Un dissettore semi-appuntito (Moria, Antony, Francia) viene utilizzato per creare un tunnel di invito nello stroma proprio partendo dal fondo della trapanazione e avanzando di 1-2 mm in senso centripeto. È facile notare una linea (piega) davanti alla punta del dissettore; la dimensione di questa linea corrisponde allo spessore del letto stromale sottostante residuo (18). A questo punto, il dissettore viene fatto avanzare nello stroma approfondendolo, fino alla riduzione dello spessore della piega e dunque alla sua scomparsa. Il dissettore viene quindi rimosso e una cannula smussata da 27 gauge (cannula di Fontana, Moria, Antony, Francia), collegata a una siringa Luer-Lock da 5 ml riempita d'aria, viene inserita nel tunnel stromale creato e fatta avanzare verso il centro della cornea per altri 2-3 mm. Mentre la cannula avanza nello stroma, il chirurgo può inizialmente percepire una certa resistenza, poi improvvisamente sopravviene una sensazione di cedimento con progressione della cannula senza sforzo: ciò indica il raggiungimento del punto desiderato per l'iniezione. L'aria viene iniettata nello stroma esercitando una decisa pressione sullo stantuffo della siringa fino alla formazione iniziale di una bolla (5-6 mm di diametro), che parte sempre dal centro della cornea e si espande centrifugamente. A questo punto l'iniezione di aria viene sospesa. Si esegue una paracentesi al limbus con un bisturi sottile per evacuare un po' di umor acqueo e ridurre la pressione intraoculare. Al seguito, l'iniezione di aria viene ripresa consentendo l'allargamento della grande bolla fino a raggiungere o superare leggermente il margine della trapanazione (8-9 mm di diametro). Se necessario, si può evacuare altro umor acqueo dalla camera anteriore per abbassare ulteriormente la pressione intraoculare.

L’aria fuoriesce dalla bolla sgonfiandosi.
La bolla si espande, occupando spazio all'interno della camera anteriore. In seguito all'infiltrazione di aria stromale (enfisema stromale), la cornea centrale diventa parzialmente bianca e opaca e la visualizzazione della camera anteriore è offuscata al centro, ma è possibile alla periferia, che di solito rimane chiara. Per confermare la presenza della bolla, si può iniettare una piccola quantità di aria nella camera anteriore attraverso una paracentesi. Quando la bolla è presente, le bolle d'aria nella camera anteriore vengono spostate in periferia dalla bolla centrale che occupa spazio. Quando non si forma la bolla, le piccole bolle d'aria che passano dalla cornea periferica attraverso la rete del trabecolato all'interno della camera anteriore si raccolgono centralmente sotto la cornea enfisematosa. Queste bolle sono libere di muoversi attraverso la camera anteriore quando l'occhio viene spostato (19). In questo caso, il chirurgo sa che la DM è rimasta attaccata allo stroma posteriore e può decidere se fare ulteriori tentativi per indurre la separazione della DM con altre iniezioni di aria o viscoelastici o cercare di esporre la DM con una tecnica di dissezione stromale strato per strato.
Nei casi in cui la formazione della bolla è riuscita, si esegue una cheratectomia lamellare anteriore per rimuovere il 30-40% della parte anteriore utilizzando un bisturi a mezzaluna (Crescent). La parete anteriore della bolla viene tagliata con un bisturi sottile, facendo collassare la bolla centrale (figura 3). Attraverso lo stesso taglio stromale, si inseriscono delle forbici corneali a punta smussata per tagliare e dividere lo stroma residuo in quattro quadranti, che vengono poi escissi tagliando lo stroma lungo il margine della trapanazione (figura 4).

Quando non si ottiene la bolla mediante la tecnica Big-Bubble, l'intervento può essere completato con la dissezione manuale del letto stromale residuo. In questo caso, dopo la rimozione di una lamella stromale anteriore, si esegue un taglio stromale radiale di circa 2 mm all'interno della zona di trapanazione, utilizzando uno strumento tagliente a piacere. Il taglio deve essere progressivamente approfondito per avvicinarsi alla DM. La progressiva dissolvenza dello stroma enfisematoso bianco e la comparsa di un riflesso scuro dell'iride attraverso lo strato traslucido della DM indicano la vicinanza di un piano stromale profondo. Una volta raggiunto un piano soddisfacente, qualsiasi strumento smusso per la dissezione stromale viene introdotto nella profondità del taglio radiale e fatto avanzare lungo lo stesso piano per separare lo stroma in senso orario o antiorario. La dissezione deve iniziare dalla metà della periferia ed estendersi oltre il margine di trapanazione, quindi verso il centro della cornea. Una volta sezionato un quadrante o più, le forbici corneali smussate vengono introdotte nella profondità della tasca per tagliare ed escindere lo stroma lungo il margine di trapanazione in modo circolare per 360 gradi. Spesso, al termine della dissezione, se la trasparenza del piano stromale residuo non è soddisfacente, è possibile eseguire una seconda dissezione circolare per ottenere una dissezione stromale profonda più vicina alla DM.
Al termine, una cornea donatrice, dello stesso diametro della trapanazione, viene punzonata dal lato endoteliale con un punch a suzione (Moria, Antony, Francia). L'endotelio e la DM vengono delicatamente rimossi mediante trazione con asciughini in merocel dopo aver colorato la superficie endoteliale con tripan blu allo 0,06% (VisionBlue; D.O.R.C., Zuidland, Paesi Bassi) per visualizzare meglio DM ed endotelio. Quattro suture cardinali interrotte in nylon 10-0 vengono utilizzate per fissare il lembo del donatore sul letto del ricevente e l'innesto viene suturato con 2 suture continue in nylon 10-0.

Le pieghe della DM si verificano spesso dopo la DALK, in particolare nei pazienti con cheratocono, a causa della DM ridondante compressa dal lembo del donatore suturato (figura 5). In questi casi, la cosiddetta tecnica di DM-tucking può essere utilizzata non appena si notano pieghe centrali della DM dopo il posizionamento dell'innesto e il tensionamento della sutura. L'epitelio del donatore viene rimosso con asciughini in merocel per evitare l’inoculo di cellule epiteliali nella giunzione lembo-ospite. Sotto pressione intraoculare fisiologica, una spatola a punta smussata (J2192.32A, E.janach, Como, Italia) viene introdotta verticalmente nel taglio di trapanazione in posizione ortogonale rispetto alla direzione principale delle pieghe della DM e fatta avanzare fino a toccare lo strato del ricevente. Mediante questo strumento, si applica una leggera pressione sufficiente a distendere lo strato della DM e a “rimboccare” lo strato pre-DM ridondante in periferia. La manovra può essere ripetuta in diversi quadranti con l'obiettivo di ottenere uno stiramento uniforme della pre-DM ridondante con raccolta verso il margine dell'innesto. La manovra viene interrotta quando si ottiene un'interfaccia donatore-ricevente regolare e non sono visibili pieghe centrali della DM (20).
1 Tan DT, Ang LP. Modified automated lamellar therapeutic keratoplasty for keratoconus: a new technique. Cornea 2006;25:1217–9.
2 Tan D, Ang LPK. Automated lamellar therapeutic keratoplasty for post-PRK corneal scarring and thinning. Am J Ophthal 2004;138:1067–1069.
3 Anwar M, Teichmann KD. Deep lamellar keratoplasty: surgical techniques for anterior lamellar keratoplasty with and without baring of Descemet’s membrane. Cornea 2002;21:374–38.
4 Anwar M, Teichmann KD. Big-bubble technique to bare Descemet’s membrane in anterior lamellar keratoplasty. J Cataract Refract Surg 2002;28:398–403.
5 Archila EA. Deep lamellar keratoplasty dissection of host tissue with intrastromal air injection. Cornea, 1984–85, 3:217–218.
6 Sujita J, Kondo J. Deep lamellar keratoplasty with complete removal of pathologic stroma for vision improvement. Br J Ophthalmol 1997;91:184–189.
7 Melles GRJ, Lander F, Rietveld FJR, et al. A new surgical technique for deep stromal, anterior lamellar keratoplasty. Br J Ophthalmol 1999;83:327–333.
8 Tsubota K, Kaido M, Monden Y, et al. A new surgical technique for deep lamellar keratoplasty with single running suture adjustment. Am J Ophthalmol 1998;126:1–8.
9 Melles GRJ, Remeijer L, Geerards AJM, et al. A quick surgical technique for deep, anterior lamellar keratoplasty using visco-dissection. Cornea 2000;19:427–432.
10 Shimmura S, Shimazaki J, Omoto M, et al. Deep lamellar keratoplasty (DLKP) in keratoconus patients using viscoadaptive viscoelastics. Cornea 2005;24:178–81.
11 Scorcia V, Busin M, Lucisano A, Beltz J, Carta A, Scorcia G. Anterior segment optical coherence tomography-guided big-bubble technique. Ophthalmology. 2013;120(3):471-476.
12 Dua HS, Faraj LA, Said DG, Gray T, Lowe J. Human corneal anatomy redefined: a novel pre-Descemet’s layer (Dua’s layer). Ophthalmology. 2013;120(9):1778-1785.
13 Fogla R. Deep anterior lamellar keratoplasty in the management of keratoconus. Indian J Ophthalmol. 2013;61(8):465-468.
14 Romano V, Iovieno A, Parente G, Soldani AM, Fontana L. Long-term clinical outcomes of deep anterior lamellar keratoplasty in patients with keratoconus. Am J Ophthalmol. 2014.
15 Jhanji V, Sharma N, Vajpayee RB. Intraoperative perforation of Descemet’s membrane during “big bubble” deep anterior lamellar keratoplasty. Int Ophthalmol. 2010;30:291–295.
16 McKee HD, Carley FM, Jhanji V, et al. Use of triamcinolone to judge needle depth in big-bubble deep anterior lamellar keratoplasty. Cornea. 2011;30:1499–1501.
17 Buzzonetti L, Laborante A, Petrocelli G. Standardized big-bubble technique in deep anterior lamellar keratoplasty assisted by the femtosecond laser. J Cataract Refract Surg. 2010;36:1631–1636.
18 Scorcia V, Lucisano A, Pietropaolo R, Savoca Corona V, Scorcia G, Busin M. Red Reflex-Guided Big-Bubble Deep Anterior Lamellar Keratoplasty: A Simple Technique to Judge Dissection Depth. Cornea. 2015 Sep;34(9):1035-8.
19 Fontana L, Parente G, Tassinari G. Simple test to confirm cleavage with air between Descemet’s membrane and stroma during big-bubble deep anterior lamellar keratoplasty. J Cataract Refract Surg. 2007 Apr;33(4):570-2.
20 Neri A, Moramarco A, Iovieno A, Fontana L. Management of Descemet Membrane’s Folds After Deep Anterior Lamellar Keratoplasty: Descemet Membrane-Tucking Technique. Cornea. 2019 Jun;38(6):772-774.
DALK: technique Big-Bubble
Abstract: Despite the long-term risk of endothelial rejection, full-thickness corneal transplantation is still considered the gold standard surgery for replacing a diseased cornea. Deep anterior lamellar keratoplasty (DALK) is not a new procedure, but in the past, its use has been of limited popularity owing to the lengthy and tedious surgery involved. With the advent of newer surgical techniques and instruments for performing lamellar corneal surgery, DALK has gained in popularity. This presentation discusses the techniques for performing the procedure as well as the clinical outcomes, especially compared with the outcomes of penetrating keratoplasty (PK). Deep anterior lamellar keratoplasty (DALK) is the logical choice in the surgical management of corneal stromal disease, in presence of a functional endothelium.